MP Biomedicals品牌商
13 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
推荐产品
公司新闻/正文
【文献解读】B. vulgatus通过调节小鼠肠道血清素合成和脂质吸收来改善高脂肪饮食诱导的肥胖
993 人阅读发布时间:2025-01-21 08:26

背景
肥胖是全球公共卫生面临的重大难题,它与多种代谢性疾病的发生、发展紧密相连[1]。多项研究表明,高脂饮食(HFD)在人类和小鼠中显著且持续地改变肠道微生物群落,导致代谢紊乱[2]。而个体的肠道微生物群落由特定的细菌谱系决定,这些谱系与消瘦或肥胖有关[3]。随着测序和分析技术的进步,越来越多的关注点转移到肥胖与肠道菌群的研究当中,致力于揭示肠道微生物群与高脂肪饮食诱导的肥胖之间的复杂联系。
摘要
在高脂饮食诱导的肥胖小鼠模型中,研究人员注意到相同月龄小鼠表现出不同的肥胖程度与代谢表型,这促使研究人员进行深入研究。结果表明,肥胖程度有别的小鼠,肠道菌群组成、结构截然不同。其中,普通拟杆菌及其代谢物胆酸,通过抑制5-羟色胺(5-HT)的合成,使非选择性阳离子通道TRPV1 活性及胞内钙水平降低,造成空肠上皮细胞脂滴积聚、乳糜颗粒滞留,最终延缓脂质吸收。这项研究展示了肠道菌群在防治代谢性疾病上的潜能,为开发新的肥胖干预靶点提供了理论依据,具有重要的应用价值。
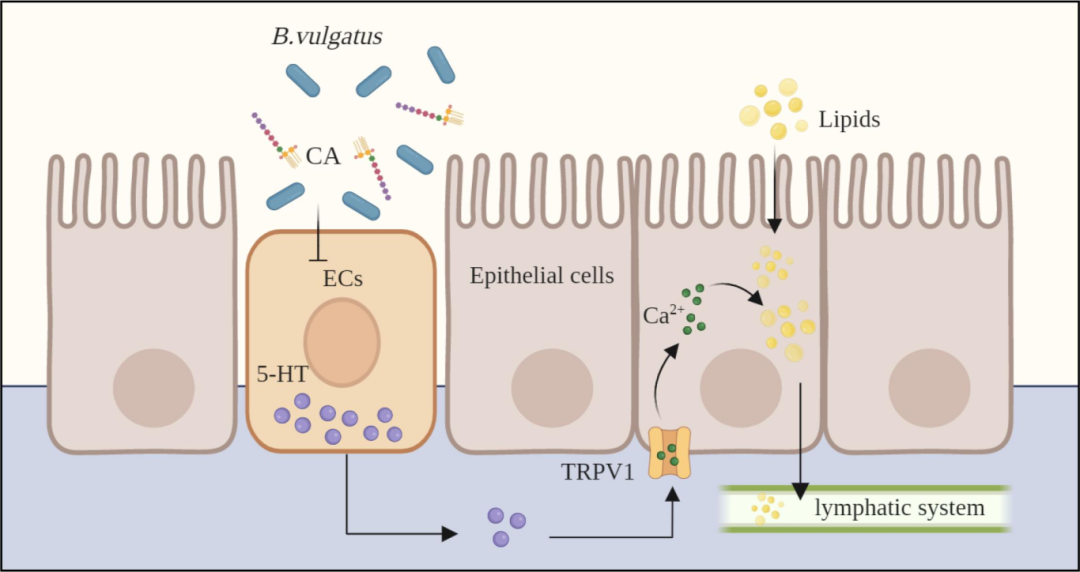
图形摘要:普通拟杆菌通过代谢物胆酸抵抗高脂饮食诱导肥胖的机制
实验流程
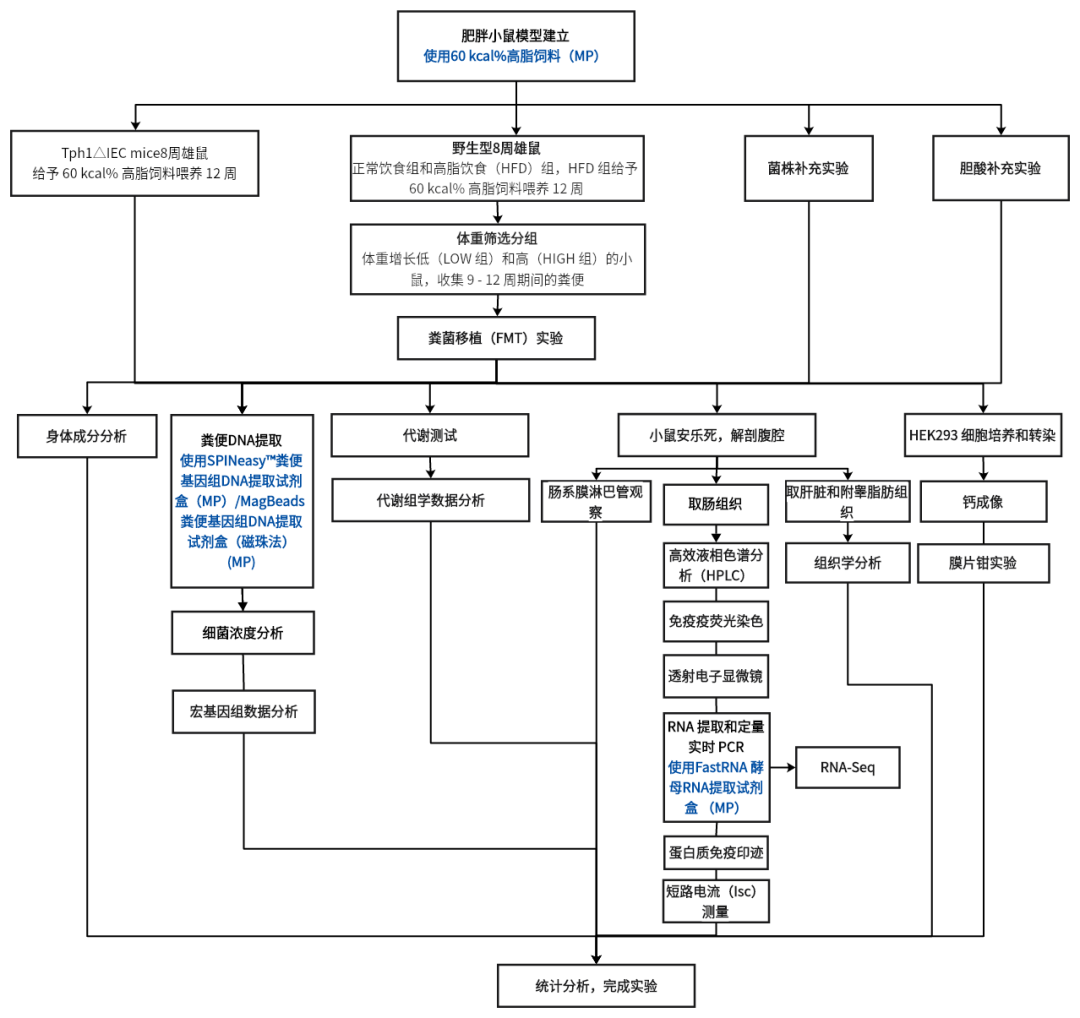
实验结果
结果1:肠道微生物群参与调节HFD诱导的肥胖
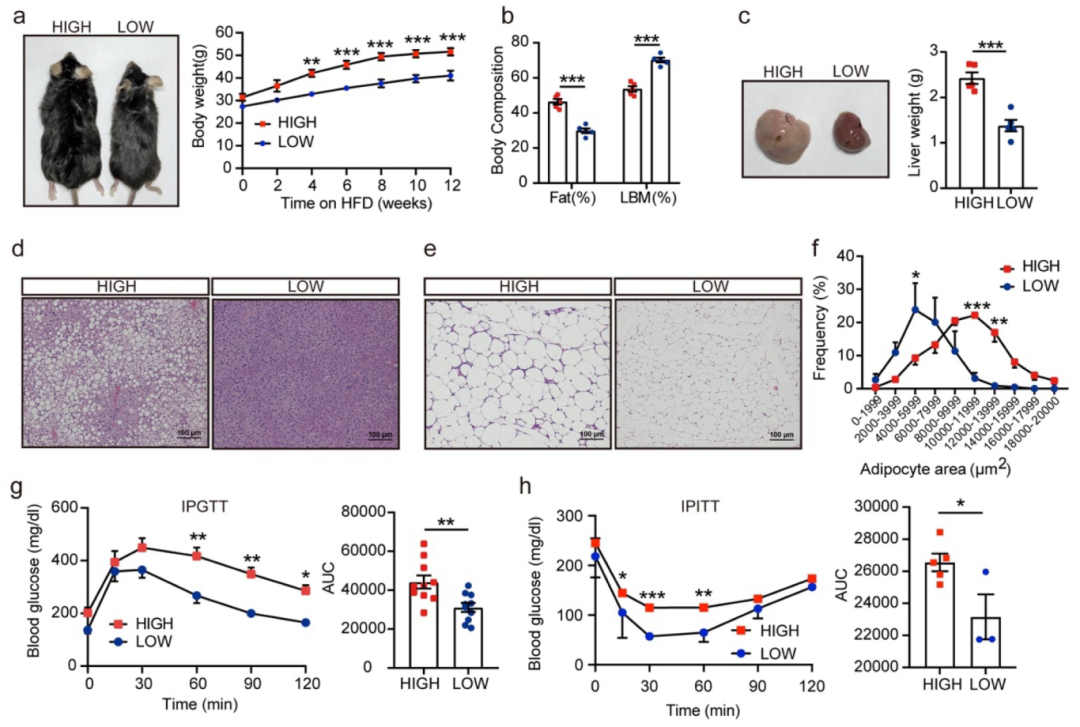
8周龄C57BL/6J小鼠经高脂饮食(HFD)诱导12周后,呈现出两种代谢表型。其中,LOW 组小鼠体重、肝脏重量显著减轻,葡萄糖耐量及胰岛素敏感性得以改善。随后,用抗生素处理 C57BL/6J 小鼠 2 周,并移植HIGH组或LOW组小鼠的粪便样本。结果发现,接受 LOW 组小鼠粪便灌胃的小鼠,在移植12周后体重增量减少,这与LOW组原本的表现一致。
结果2:B.vulgatus 减轻 HFD 诱导的肥胖
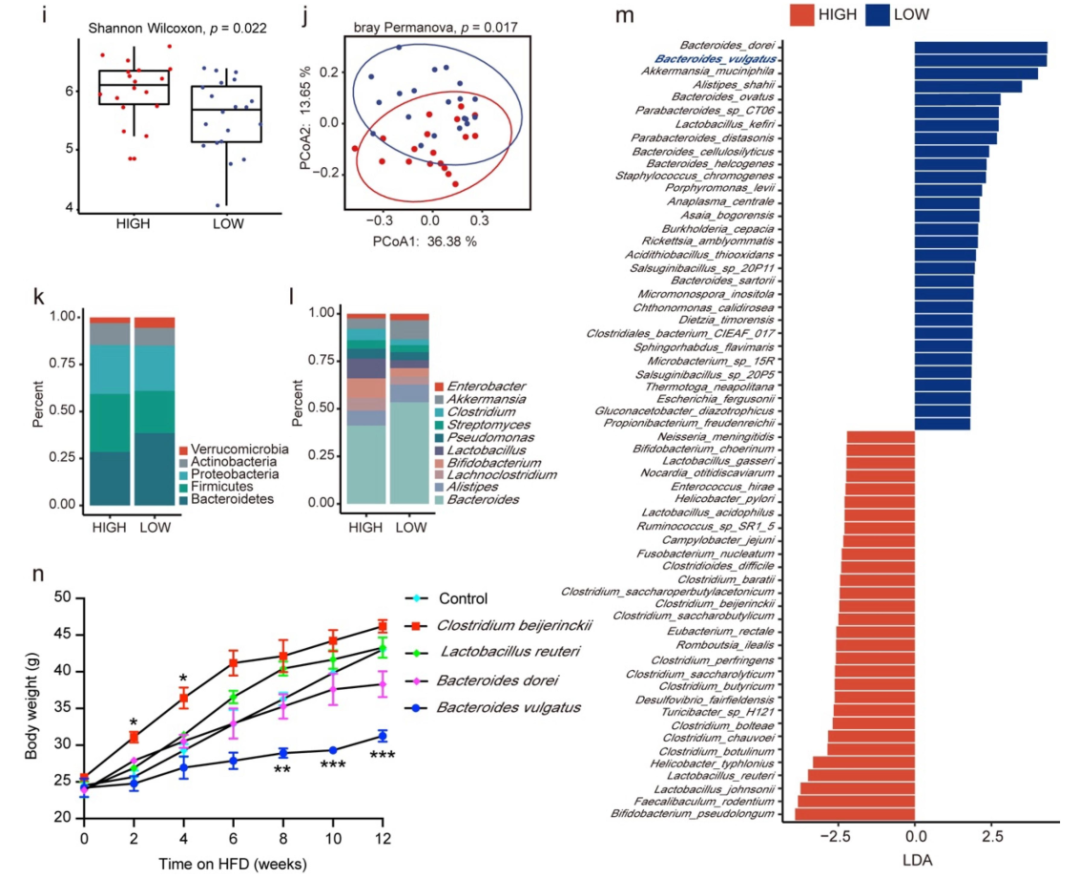
使用HIGH组和LOW组小鼠的粪便样本开展宏基因组测序,发现相较于LOW 组小鼠,HIGH 组小鼠的 Firmicutes(厚壁菌门)/Bacteroidetes(拟杆菌门)比率显著升高。从属水平来看,LOW组小鼠拟杆菌属丰度显著增多,而 HIGH 组小鼠乳杆菌属丰度显著增加。进一步通过 LEfSe分析可知,LOW组中B.dorei和B.vulgatus是关键菌种,同时在HIGH组中梭状芽孢杆菌属、乳杆菌属中的L. reuteri显著增多。
为判断这些特定菌株能否治疗或诱导肥胖,将上述四种菌灌胃给小鼠。结果表明,定植B. vulgatus的小鼠体重明显低于对照组小鼠,而定植C. beijerinckii的小鼠则呈现出体重增加的趋势。
结果3:微生物的代谢物胆酸可预防HFD诱导的肥胖
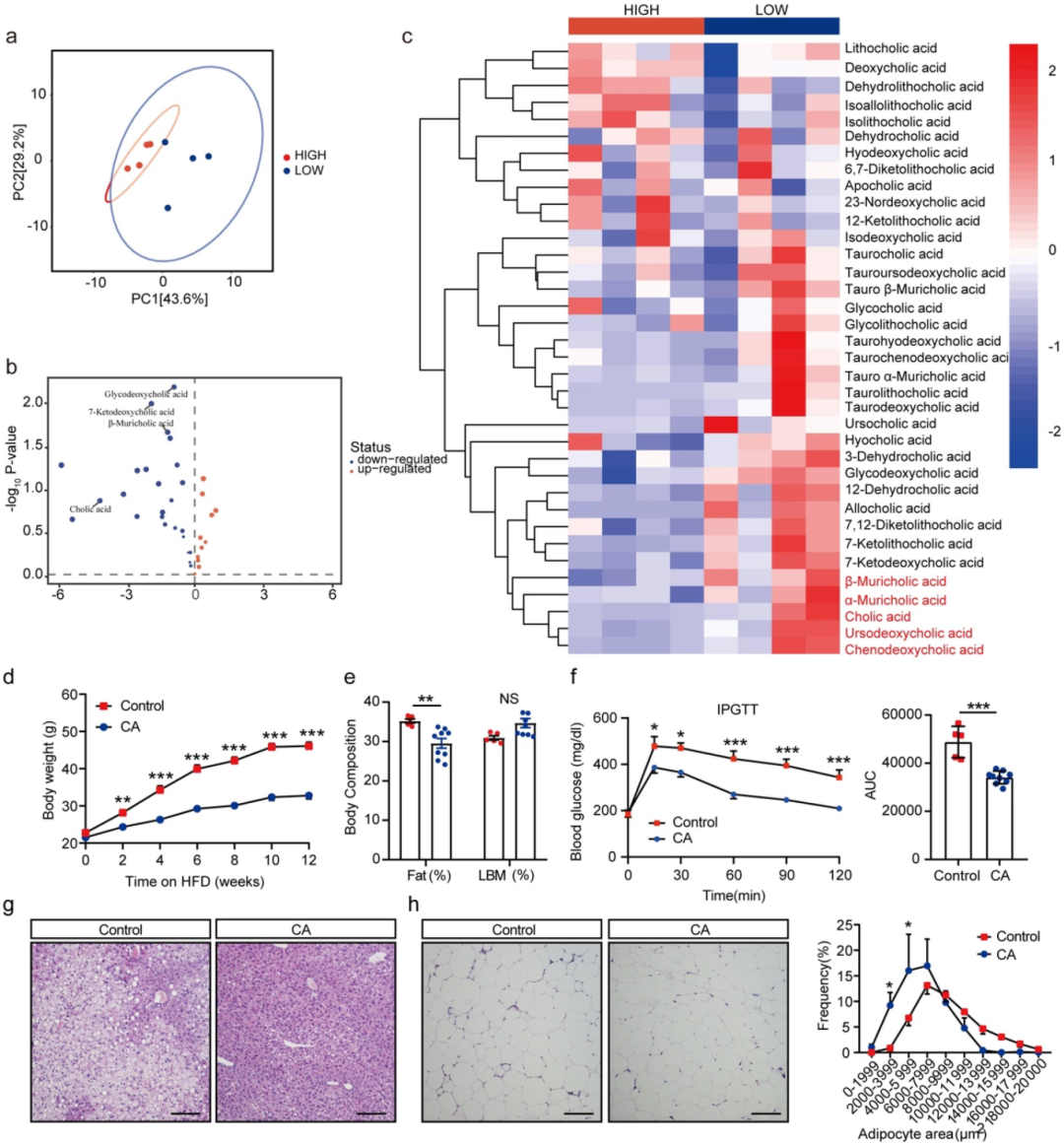
利用超高效液相色谱串联质谱法(UHPLC-MS/MS)对 HIGH 组与 LOW 组小鼠的粪便代谢物进行检测,经火山图分析后,锁定胆酸(CA)、β-MCA、7 - 酮 - 3α,12-α- 羟基胆烷酸以及甘氨脱氧胆酸作为能够区分两组小鼠的候选标记物。为深入探究 CA 的具体作用,在高脂饮食(HFD)中额外添加CA,结果显示,小鼠体重增长幅度减小,脂肪体质量占比降低。
结果4:肠道菌群调节肠道脂质吸收以减少 HDF 诱导的肥胖
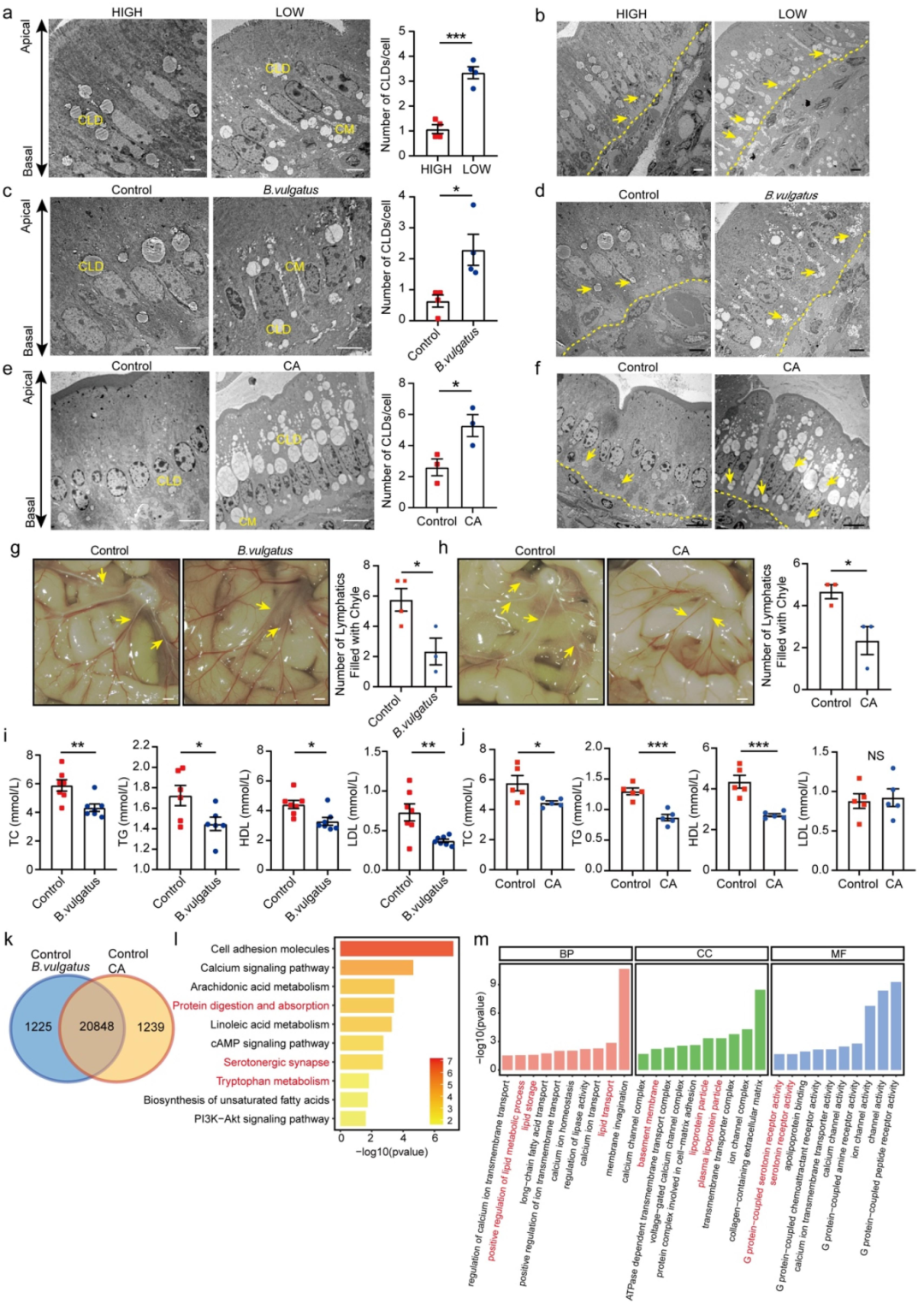
通过透射电子显微镜(TEM)观察小鼠肠上皮细胞内的脂质转运情况。对比 HIGH 组小鼠,LOW 组小鼠肠上皮细胞中有明显的乳糜颗粒积聚现象。在定植B. vulgatus或者补充胆酸(CA)的小鼠体内,空肠肠系膜对乳糜微粒的摄取显著减少,这意味着脂质的基底外侧转运速率减慢,使得高脂饮食摄入后脂质吸收过程延迟。不仅如此,相较于对照组,这些小鼠血清中的血脂水平也显著降低,充分表明肠道微生物群能够阻碍空肠中的乳糜颗粒向乳糜管运输。研究人员提取了对照组以及定植B. vulgatus或补充 CA 的小鼠空肠上皮 mRNA 进行转录组测序,通过 MF 富集分析发现,差异表达基因集中在 G 蛋白偶联的 5 - HT受体以及 5 -HT受体活性相关途径,这提示乳糜颗粒转运减少很可能与 5-HT存在紧密联系。
研究结论
该研究揭示了与高脂饮食相关的肠道微生物代谢调节肠道5-HT合成,这对宿主的脂质吸收至关重要。作者证实了脆弱拟杆菌和代谢产物胆酸通过抑制EC细胞中的5-HT合成来减少HFD诱导的肥胖,并且创新性地发现5-HT通过激活TRPV1增加了肠道上皮细胞内钙,从而促进脂质吸收。这项研究成功揭示出一条全新的信号传导轴,即微生物群落 - 代谢物 - 5-HT 与脂质吸收之间的紧密联系,为攻克 HFD 诱导的肥胖难题提供了极具潜力的治疗靶点,有望开辟新的治疗路径。
参考文献:
[1] Wang Y, Zhao L, Gao L, et al. Health policy and public health implications of obesity in China. Lancet Diabetes Endocrinol. 2021;9(7):446–461.
[2] Marchesi JR, Adams DH, Fava F, et al. The gut microbiota and host health: a new clinical frontier. Gut. 2016;65(2):330–339.
[3] Aron-Wisnewsky J, Warmbrunn MV, Nieuwdorp M, et al Metabolism and metabolic disorders and the microbiome: the intestinal microbiota associated with obesity, lipid metabolism, and metabolic health_x0002_pathophysiology and therapeutic strategies. Gastroenterology. 2021;160(2):573–599.